二氧化锰
二氧化锰eryanghuameng
化学式MnO2,是最常见的锰 (Ⅵ) 化合物,是自然界中软锰矿的主要成分。它是灰黑色粉未状固体,相对密度为5.026,加热至535℃时分解放氧。不溶于水、硝酸、冷硫酸,是两性氧化物。但碱性与酸性都较弱。其酸性表现于与强碱或碱性氧化物熔融得MnO2-3,如:

MnO2+4HCl=Cl2+MnCl2+2H2O
这也说明锰 (Ⅳ) 盐在酸性介质中不如锰 (Ⅱ) 稳定。二氧化锰与浓硫酸作用得硫酸锰并放出氧气: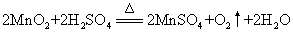
二氧化锰在碱性介质中有氧化剂 (如空气中氧或氯酸钾等) 存在的条件下,也可表现出还原性,例如:
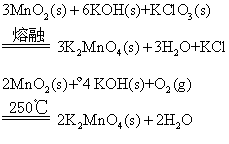
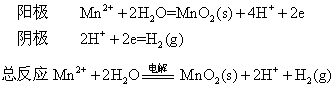
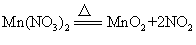
也可以天然软锰矿为原料来制取。
☚ 锰 氢氧化锰 ☛
二氧化锰
manganese dioxide
- 小丁香是什么意思
- 小丁香丸是什么意思
- 小丁香丸是什么意思
- 小丁香丸是什么意思
- 小丁香散是什么意思
- 小丁香煎是什么意思
- 小七气汤是什么意思
- 小七香丸是什么意思
- 小七香丸是什么意思
- 小七香丸是什么意思
- 小七香丸是什么意思
- 小七香丸是什么意思
- 小七香丸是什么意思
- 小万卷斋诗稿是什么意思
- 小万卷楼是什么意思
- 小万卷楼丛书是什么意思
- 小万年草是什么意思
- 小三五七散是什么意思
- 小三分家是什么意思
- 小三叶耳蕨是什么意思
- 小三叶耳蕨是什么意思
- 小三弦是什么意思
- 小三棱煎是什么意思
- 小三棱煎是什么意思
- 小三棱煎丸是什么意思
- 小三棵针是什么意思
- 小三生丹是什么意思
- 小三颗针是什么意思
- 小三颗针是什么意思
- 小三黄汤是什么意思
- 小不忍则乱大谋是什么意思
- 小不忍则乱大谋是什么意思
- 小不忍则乱大谋是什么意思
- 小不忍则乱大谋是什么意思
- 小不点儿的冒险故事是什么意思
- 小丑是什么意思
- 小丑之夜是什么意思
- 小丑汉斯是什么意思
- 小丑皇帝是什么意思
- 小世界是什么意思
- 小世界是什么意思
- 小业主是什么意思
- 小东是什么意思
- 小东西是什么意思
- 小丝片平衡是什么意思
- 小丝片疵点是什么意思
- 小丝片给湿是什么意思
- 小丝片给湿助剂是什么意思
- 小丝片给湿机是什么意思
- 小丫头是什么意思
- 小中取大准则是什么意思
- 小中取大法决策是什么意思
- 小中风是什么意思
- 小中风是什么意思
- 小串是什么意思
- 小丹搨方是什么意思
- 小主人半月刊是什么意思
- 小主语是什么意思
- 小乌头丸是什么意思
- 小乌沉汤是什么意思