卤化磷
卤化磷luhualin
磷与卤素形成的化合物及其衍生物。二元磷卤化物通常有两种类型——三卤化磷PX3和五卤化磷PX5,但碘形成三碘化磷和四碘化二磷。三卤化磷分子结构与氨或瞵相似,磷原子为sp3杂化,分子形状为三角锥形,磷原子位于角顶,有一对孤电子对。在平常条件下三氟化磷为无色气体,三氯化磷与三溴化磷为无色挥发性液体,三碘化磷为暗红色低熔点固体。三卤化磷中以三氟化磷为最稳定,并且化学性质不活泼,由三氟化磷到三碘化磷稳定性下降,这与P—X键能所表明的规律一致。例如,三氟化磷与水反应很慢,而三氯化磷则迅速水解:
PCl3+3H2O=H2PHO3+3H++3Cl-
在三卤化磷中,磷原子有 一对孤电子对,易与电子对接受体的化合物作用,例如,三氯化磷与三氯化硼反应可形成低熔点的固体PCl3·BCl3。三卤化磷与卤素作用可得磷 (V) 的卤化物:PCl3+Cl2=PCl5
在通常条件下,五氟化磷为无色气体,五氯化磷为无色固体,五溴化磷为黄色或红色固体。五卤化磷的热稳定性从五氟化磷到五溴化磷依次下降,五氯化磷热分解反应曾作为可逆反应的突出例子而被人们详细研究过: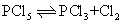
PX5+4H2O=H3PO4+5HX
在非水溶液中,五氟化磷可与碱性氟化物作用:KF+PF5=KPF6
三卤化磷不仅可与卤素单质作用,也可与氧作用,生成磷 (V) 的卤氧化物POX3,如:
PCl3+1/2O2=POCl3 (磷酰氯)
☚ 次磷酸 砷 ☛
- 沈幾是什么意思
- 沈广祚是什么意思
- 沈庄是什么意思
- 沈庄子是什么意思
- 沈庄子街道办事处是什么意思
- 沈庆之是什么意思
- 沈庆之哭市救人是什么意思
- 沈庆云是什么意思
- 沈庆京是什么意思
- 沈应是什么意思
- 沈应乾是什么意思
- 沈应元是什么意思
- 沈应召是什么意思
- 沈应善是什么意思
- 沈应时是什么意思
- 沈应明是什么意思
- 沈应瑞是什么意思
- 沈应科是什么意思
- 沈应魁是什么意思
- 沈庚斋是什么意思
- 沈府君神道闕是什么意思
- 沈府君闕是什么意思
- 沈府君阙是什么意思
- 沈度是什么意思
- 沈度寫真像 明_名典輔文是什么意思
- 沈度明是什么意思
- 沈度楷书敬斋箴是什么意思
- 沈度楷书敬斋箴页是什么意思
- 沈庭煜是什么意思
- 沈庭訓是什么意思
- 沈庭训是什么意思
- 沈庵是什么意思
- 沈康辰是什么意思
- 沈庸是什么意思
- 沈廛是什么意思
- 沈延世是什么意思
- 沈延国是什么意思
- 沈延太是什么意思
- 沈延毅是什么意思
- 沈廷文是什么意思
- 沈廷正是什么意思
- 沈廷炤是什么意思
- 沈廷璐是什么意思
- 沈廷芳是什么意思
- 沈廷钟是什么意思
- 沈廷镛是什么意思
- 沈廷颺是什么意思
- 沈建是什么意思
- 沈建华是什么意思
- 沈建南是什么意思
- 沈建图是什么意思
- 沈开基是什么意思
- 沈开木是什么意思
- 沈开樾是什么意思
- 沈开荣是什么意思
- 沈弘先是什么意思
- 沈弼是什么意思
- 沈弼和是什么意思
- 沈归愚是什么意思
- 沈归愚全集是什么意思