硝酸的氧化性
硝酸的氧化性xiaosuan de yanghuaxing
硝酸是一种常见的氧化性酸,它具有较强氧化性的原因是,硝酸中的氮元素处在最高价,且硝酸分子不稳定,能分解出氧气和二氧化氮。它在反应中可被还原成二氧化氮、亚硝酸、一氧化氮、氧化二氮、氨气 (在酸性条件下形成铵盐) 等。硝酸的还原产物与本身的浓稀及还原剂的强弱有关,一般情况下,浓硝酸被还原成二氧化氮,稀硝酸被还原成+2价以下的物质,酸的浓度越稀,还原剂越强,被还原的程度越大。例如:
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
4Zn+10HNO3(稀)=4Zn(NO3)2+N2O↑+5H2O
4Mg+10HNO3 (很稀)
=4Mg(NO3)2+NH4NO3+3H2O
硝酸参加的主要氧化-还原反应:
❶硝酸几乎可以和一切金属作用 (除金、铂、铱等) ,例如:

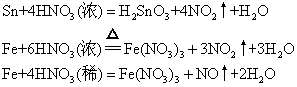
❷具有还原性的非金属单质可被硝酸氧化,例如:

❸具有还原性的化合物可被硝酸氧化,例如:
3Cu2S+22HNO3
=6Cu(NO3)2+10NO↑+3H2SO4+8H2O
10HNO3+3FeO=3Fe(NO3)3+NO↑+5H2O
3As2O3+4HNO3+7H2O=6H3AsO4+4NO↑
3Na2SO3+2HNO3=3Na2SO4+2NO↑+H2O
3BaSO3+2HNO3=3BaSO4+2NO↑+H2O
☚ 浓硫酸的氧化性 王水的氧化性 ☛
- 高雪病是什么意思
- 高雪病是什么意思
- 高雪轮是什么意思
- 高雷人民抗日军是什么意思
- 高雷片(系)是什么意思
- 高震中是什么意思
- 高霞堂集是什么意思
- 高青是什么意思
- 高青县志是什么意思
- 高静山是什么意思
- 高静山是什么意思
- 高静山是什么意思
- 高静熙是什么意思
- 高顶簇盘是什么意思
- 高顺是什么意思
- 高颎是什么意思
- 高颎是什么意思
- 高颎是什么意思
- 高颎(音炯jiǒng)是什么意思
- 高颐墓阙及石刻是什么意思
- 高颐阙是什么意思
- 高频、微波功率的计量测试是什么意思
- 高频、微波场强与干扰的计量测试是什么意思
- 高频喷射通气是什么意思
- 高频对称电缆反耦合网络手册是什么意思
- 高频开关稳压电源是什么意思
- 高频心电图是什么意思
- 高频心电图是什么意思
- 高频振框筛平衡是什么意思
- 高频放大器是什么意思
- 高频时变信道是什么意思
- 高频烘箱是什么意思
- 高频率相控阵多普勒声雷达是什么意思
- 高频率节奏是什么意思
- 高频瓷的电气物理基础是什么意思
- 高频电压的计量测试是什么意思
- 高频电场烘茧是什么意思
- 高频电子线路是什么意思
- 高频电子线路是什么意思
- 高频电子线路是什么意思
- 高频电流干燥方法是什么意思
- 高频电疗法是什么意思
- 高频电路是什么意思
- 高频电路基础是什么意思
- 高频通气是什么意思
- 高频部分是什么意思
- 高额垄断利润是什么意思
- 高风是什么意思
- 高风亮节是什么意思
- 高风亮节是什么意思
- 高风亮节是什么意思
- 高风亮节是什么意思
- 高风以低兮,览周流于朔方。是什么意思
- 高风催节变,凝露督物化。长林悲素秋,茂草思朱夏。是什么意思
- 高风内障是什么意思
- 高风雀目内障是什么意思
- 高风雀目内障是什么意思
- 高飞是什么意思
- 高飞之鸟,死于美食;深泉之鱼,死于芳饵是什么意思
- 高飞远举是什么意思