硼酸boron acid
用碳酸氢铵处理硼镁矿粉或用硫酸中和硼砂等方法制成的硼肥。化学式为HBO3。含硼量(B)17.5%。白色结晶或白色粉末,溶于水,呈弱酸性,不吸湿。可作基肥、追肥、种肥施用。但以用于根外追肥较为经济有效。作根外追肥的喷施浓度为0.1%~0.2%,溶液用量以喷湿叶片正反面为度。作拌种用时,每500 g种子只需用硼酸0.2~0.5 g;浸种用的硼酸溶液浓度为0.01%~0.05%。
硼酸
硼酸pengsuan
硼的氧化物水合物。主要有四硼酸H2B4O7,偏硼酸 (HBO2)n与正硼酸H3BO3 (也称原硼酸) ,其中正硼酸含水量最多,最稳定。正硼酸也简称硼酸,它是白色发亮的片状晶体,0℃时溶解度为2.6g,107℃时溶度为37g,故可用重结晶法提纯。用硫酸作用于硼砂解的热溶液可制得硼酸:
Na2B4O7+H2SO4+5H2O=Na2SO4+4H3BO3
我国东北有丰富的硼镁矿MgB2O5· H2O或2MgO·B2O5·H2O。直接用硫酸分解硼镁矿也可制得硼酸:
Mg2B2O5·H2O+2H2SO4=2MgSO4+2H3BO3
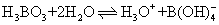
这与硼化合物缺电子结构特点有关,硼酸中硼原子可作为电子对接受体与一个OH-根结合,OH-根中

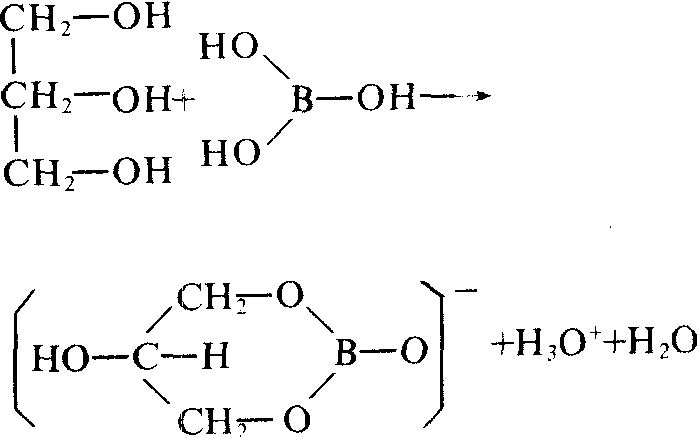
典型的路易斯酸。当硼酸中加入甘油 (丙三醇)或甘露醇[CH2(OH)(CHOH)4CH2OH]时,其酸性增强,这是因为硼酸与甘油结合生成配阴离子后,将H+推到外界,易于电离:
H3BO3+3C2H5OH=B(OC2H5)3+3H2O
根据这一反应原理可使硼酸或硼酸盐从酸溶性矿物中分离出来。硼酸三甲酯 (或硼酸三乙酯) 燃烧时,生成绿色火焰,利用这一特性可定性地鉴定硼酸或其盐的存在。硼酸水溶液具有弱酸性和杀菌能力,在医药和食品工业、造纸和制革工业上用做消毒剂和防腐剂,硼酸也用于搪瓷和釉药的制造,也是制造玻璃纤维的重要原料之 一。☚ 氧化硼 硼酸盐 ☛
硼酸boric acid
系一种外用消毒剂。其制剂有3%溶液、2%醑剂、10%软膏。本品刺激性小,3%溶液可用于眼、口腔、膀胱、子宫冲洗;也可用皮肤湿疹等处湿敷。本品禁内服。
硼酸
boric acid
硼酸
boric acid
硼酸
boric acid
硼酸
boric acid
~盐borate
- 基本有机合成工艺学是什么意思
- 基本有机合成理论基础是什么意思
- 基本本体论是什么意思
- 基本权利是什么意思
- 基本权利是什么意思
- 基本条款是什么意思
- 基本标准成本是什么意思
- 基本标准成本是什么意思
- 基本核算单位是什么意思
- 基本核算单位是什么意思
- 基本概念是什么意思
- 基本概念是什么意思
- 基本概念是什么意思
- 基本款目是什么意思
- 基本母畜是什么意思
- 基本汇率是什么意思
- 基本汇率是什么意思
- 基本汇率是什么意思
- 基本治疗是什么意思
- 基本法是什么意思
- 基本法是什么意思
- 基本法律❶ 是什么意思
- 基本消费资料是什么意思
- 基本焦虑是什么意思
- 基本物价方程式是什么意思
- 基本生产是什么意思
- 基本生产和辅助生产是什么意思
- 基本(生产)工人劳动生产率分析是什么意思
- 基本生活设施完善度资料整理是什么意思
- 基本电价是什么意思
- 基本电路理论是什么意思
- 基本的宏观经济模型是什么意思
- 基本的是游击战 但不放松有利条件下的运动战是什么意思
- 基本矛盾是什么意思
- 基本矛盾是什么意思
- 基本矛盾是什么意思
- 基本确定年金是什么意思
- 基本社群是什么意思
- 基本空气动力学是什么意思
- 基本等级是什么意思
- 基本粒子是什么意思
- 基本粒子是什么意思
- 基本粒子是什么意思
- 基本粒子是什么意思
- 基本粒子发现简史是什么意思
- 基本粒子相互转化是什么意思
- 基本经济规律是什么意思
- 基本经济规律是什么意思
- 基本经济规律是什么意思
- 基本经济规律是什么意思
- 基本经济规律是什么意思
- 基本群是什么意思
- 基本药物临床评价是什么意思
- 基本薄膜厚度的模口范围是什么意思
- 基本计算是什么意思
- 基本设计:视觉形态动力学是什么意思
- 基本证据是什么意思
- 基本词汇是什么意思
- 基本词汇是什么意思
- 基本词汇和一般词汇是什么意思