配离子的不稳定常数
配离子的不稳定常数peilizi de buwending changshu
配离子在溶液中存在离解与配位平衡,如

其离解也是分步进行的,与多元酸碱多级电离类似。离解平衡与弱电解质电离平衡相似,也可写出配离子的离解平衡常数
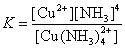
K值越大,表示CuNH32+4配离子越易离解,即配离子越不稳定。因此,配离子的离解常数K也称为[Cu(NH3)4]2+配离子的不稳定常数,符号记作K不稳,它是配离子的特征常数。不同的配离子有不同的不稳定常数,如[Cu(NH3)4]2+的K不稳为2.09×10-13,[Cd(NH3)4]2+的K不稳为2.75×10-7,[Zn(NH3)4]2+的K不稳为2.00×10-9。根据K不稳值越大,配离子越不稳定,即越易离解,得出它们在溶液中的稳定性顺序为
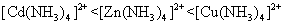
配离子在溶液中的稳定性还可用稳定常数表示,
如CuNH3)4]2+配离子的生成反应
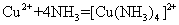
其平衡常数为

K值越大,表示生成配离子的倾向越大,则配离子离解的倾向就越小,即配离子越稳定。因此,配离子的生成常数又叫[Cu(NH3)4]2+的稳定常数,可用K稳表示。不同的配离子,其稳定常数是不同的。稳定常数的大小,直接反映配离子稳定性的大小。显然,K不稳与K稳互为倒数的关系,即
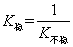
应用时需要注意。常温下一些常见配离子的稳定常数见下表。
一些常见配离子的稳定常数
| 配离子 | K稳 | 配离子 | K稳 |
| 1:2 [Cu(NH3)2]+ [Cu(CN)2]- [Ag(NH3)2]+ [Ag(en)2]+ [Ag(CNS)2]- [Ag(CN)2]- [Cu(en)2]2+ [Ag(S2O3)2]3- 1:4 | 7.4×1010 2.0×1038 1.7×107 7.0×107 4.0×108 1.0×1021 4.0×1019 1.6×1013 | [Zn(CNS)4]2- [Zn(CN)4]2- [Cd(CNS)4]2- [Cd(CN)4]2- 1:6 | 2.0×101 1.0×1016 1.0×103 1.3×1018 |
| [Cd(NH3)6]2+ [Co(NH3)6]2+ [Ni(NH3)6]2+ [Co(NH3)6]3+ [Fe(CN)6]3- [Fe(CN)6]4- [Co(CN)6]3- [FeF6]3- | 1.4×106 2.4×104 1.1×108 1.4×1035 1×1042 1×1035 1×1064 1.0×1016 | ||
| [Cu(NH3)4]2+ [Zn(NH3)4]2+ [Cd(NH3)4]2+ | 4.8×1012 5×108 3.6×106 |
☚ 溶度积 电离理论 ☛
- 《五美吟(其三)》是什么意思
- 《五美吟(其二)》是什么意思
- 《五美吟(其五)》是什么意思
- 《五美吟(其四)》是什么意思
- 《五美吟(黛玉)》是什么意思
- 《五美缘》是什么意思
- 《五脏论》写本是什么意思
- 《五色令人目盲》是什么意思
- 《五色石》是什么意思
- 《五芳斋·名家·本地姜》是什么意思
- 《五虎平南后传》是什么意思
- 《五虎平西前传》是什么意思
- 《五蠹》是什么意思
- 《五蠹(节选)》是什么意思
- 《五重塔》是什么意思
- 《五鼠闹东京包公收妖传》是什么意思
- 《五)(小草在歌唱——悼女共产党员张志新烈士)(雷抒雁)是什么意思
- 《井州歌》是什么意思
- 《井底引银瓶》是什么意思
- 《井)(杜运燮)是什么意思
- 《亚细亚》被炸是什么意思
- 《亚细亚报》馆爆炸案是什么意思
- 《亡人》是什么意思
- 《亡友鲁迅印象记》读后记是什么意思
- 《亡妻龚氏圹铭》是什么意思
- 《亡妻龚氏圹铭》 - 〔清〕彭绩是什么意思
- 《亡灵书》是什么意思
- 《交响曲》是什么意思
- 《交若侪辈 姜宸英 方苞》是什么意思
- 《交际花盛衰记》是什么意思
- 《亦不见佳 宋琬》是什么意思
- 《亦嫁彭郎 毛藻 罗恕》是什么意思
- 《亨利四世》是什么意思
- 《亨利第四》是什么意思
- 《京华烟云》是什么意思
- 《京口作》 - 清·叶燮是什么意思
- 《京口月夕书怀》是什么意思
- 《京口耆旧传》是什么意思
- 《京师为包拯语》是什么意思
- 《京师为童贯蔡京高俅何执中谣》是什么意思
- 《京师乐籍说》 - 〔清〕龚自珍是什么意思
- 《京师人为严嵩语》是什么意思
- 《京本通俗小说》是什么意思
- 《京都大学人文科学研究所藏甲骨文·本文篇》是什么意思
- 《京都谣》是什么意思
- 《亮公房雨后》是什么意思
- 《亲戚》是什么意思
- 《亲擢首选 赵构 张孝祥 秦桧》是什么意思
- 《亲政篇》是什么意思
- 《亲爱的,别把我的信揉成一团》是什么意思
- 《亲爷娶晚妻》是什么意思
- 《亲老婆》是什么意思
- 《人与时)(鲁迅)是什么意思
- 《人世百图》后记是什么意思
- 《人世间》是什么意思
- 《人中画》是什么意思
- 《人京》 - 明·于谦是什么意思
- 《人人劝我》是什么意思
- 《人伦之变 陆游》是什么意思
- 《人儿人儿今何在》是什么意思