酸式盐与酸、碱的反应
酸式盐与酸、碱的反应jian de fanyingsuanshiyan yu suan
强酸的酸式盐在水中可电离出全部氢离子,例如:
NaHSO4=Na++H++SO2-4
因此它具有较强的酸性,能与碱发生中和反应,生成水和正盐,例如:
NaHSO4+NaOH=Na2SO4+H2O
2KHSO4+2NH3·H2O
=K2SO4+(NH4)2SO4+2H2O
2NaHSO4+Cu(OH)2=Na2SO4+CuSO4+2H2O
弱酸的酸式盐在水中的电离分步进行,例如:
NaHCO3=Na++HCO-3
HCO-3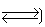 H++CO2-3
H++CO2-3
NaHCO3+NaOH=Na2CO3+H2O
2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑
NaHS+HCl=NaCl+H2S↑
Ca(H2PO4)2+H2SO4=CaSO4↓+2H3PO4
(NH4)2HPO4+H3PO4=2NH4H2PO4
弱酸酸式盐的溶解性一般比相应的正盐好,因此在它与碱反应时,常伴随着沉淀生成,例如:
Ca(HCO3)2+2NaOH (过量)
=CaCO3↓+Na2CO3+2H2O
HCO-3+OH-=CO2-3+H2O
CO2-3+Ca2+=CaCO3↓
Mg(HCO3)2+2Ca(OH)2
=Mg(OH)2↓+2CaCO3↓+2H2O
Mg2++2OH-=Mg(OH)2↓
HCO-3+OH-=CO2-3+H2O
2CO2-3+2Ca2+=2CaCO3↓
☚ 酸式盐的生成 铝与强碱溶液的反应 ☛
- 用户调查预测法是什么意思
- 用户费是什么意思
- 用户集中器是什么意思
- 用户驻地网是什么意思
- 用才方法是什么意思
- 用扩散管作为采集气态组分的工具是什么意思
- 用抓斗式起重机装车及卸车是什么意思
- 用拳头骨干去打击敌人是什么意思
- 用推板式卸车机卸车是什么意思
- 用文尚能是什么意思
- 用文斗,不用武斗是什么意思
- 用新党章教育党员,为整党做好思想准备是什么意思
- 用新的态度对待新的劳动是什么意思
- 用易详解是什么意思
- 用易详解是什么意思
- 用是是什么意思
- 用晦是什么意思
- 用晦是什么意思
- 用智是什么意思
- 用替代字是什么意思
- 用木版活字出版《孝经》是什么意思
- 用李萨如图形分析振动是什么意思
- 用材不当是什么意思
- 用材林是什么意思
- 用材林产品成本是什么意思
- 用武是什么意思
- 用武之地是什么意思
- 用水废水化学基础是什么意思
- 用水总量的计算是什么意思
- 用水权是什么意思
- 用水泥、石灰、沥青和煤沥青加固土铺筑道路底层和面层的现代化方法是什么意思
- 用水管理是什么意思
- 用汽的特点是什么意思
- 用汽负荷的确定是什么意思
- 用法是什么意思
- 用清是什么意思
- 用激光测定回转窑中心线是什么意思
- 用热远热是什么意思
- 用瓦·西汤(姜黄四味汤)是什么意思
- 用电最大负荷是什么意思
- 用电管理与监察是什么意思
- 用电管理培训教材是什么意思
- 用电管理工作手册是什么意思
- 用电管理文书是什么意思
- 用电设备的避雷针保护范围计算是什么意思
- 用益权是什么意思
- 用益权制度是什么意思
- 用益物权是什么意思
- 用益物权是什么意思
- 用益物权是什么意思
- 用盐核销定额是什么意思
- 用相互独立的双超声束多普勒效应定量测定血流速度是什么意思
- 用短与用长是什么意思
- 用硫率的计算是什么意思
- 用碱量和用水量是什么意思
- 用神是什么意思
- 用神是什么意思
- 用神不现是什么意思
- 用神两现是什么意思
- 用神六亲是什么意思