
称三氯化铁、氯化铁(Ⅲ)。
有无水物、六水合物、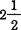 、2及3水合物。常见者为无水物[1]及六水合物[2]。
、2及3水合物。常见者为无水物[1]及六水合物[2]。
(1)[1]为六方晶系暗红紫色叶片状晶体。有潮解性。相对分子质量162.22。相对密度2.898(25℃)。
熔点306℃。沸点315℃(升华)。
在440℃成为二聚物。
高于此温度则分解,放出氯。难溶于苯,微溶于二硫化碳,易溶于乙醇、乙醚、丙酮、甘油、吡啶、苯基氰、硫酰氯,溶于水:0℃时74.4、10℃时81.8、20℃时96.9、25℃时99、30℃时282、50℃时315、60℃时373、80℃时526、100℃时536。在氢气流中加热最初生成氯化亚铁,然后变为铁。
在氧气流中加热则生成Fe2O3和氯气。大鼠经口LD50900mg/kg。
用途:有机反应的氯化剂、缩合剂及氯化反应催化剂及氧化剂;金属板蚀刻剂、印刷电路版蚀刻剂;媒染剂;水处理剂;其他铁盐原料、颜料及医药止血剂;食品添加剂,用作铁质强化剂。使用最多者为无水物。
(2)[2]为六方晶系黄褐色晶体或橙色单斜晶体。有盐酸气味。
易潮解。相对密度1.82。熔点36.5℃。沸点280~285℃。溶于水(20℃时91.9),水溶液因水解而呈黄褐色,也溶于乙醇、乙醚和丙酮。具有反式[FeCl2(H2O)4]Cl·2H2O结构。
水溶液呈酸性。对蛋白质起凝固作用。
(3)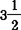 水合物[FeCl3·
水合物[FeCl3·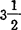 H2O]比六水合物颜色更暗,单斜晶系结晶。熔点32.5℃。
H2O]比六水合物颜色更暗,单斜晶系结晶。熔点32.5℃。
(4)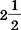 水合物[FeCl3·
水合物[FeCl3·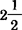 H2O]呈黄红色。斜方晶系结晶。
H2O]呈黄红色。斜方晶系结晶。
熔点56℃。溶于水、乙醇和乙醚。
(5)二水合物[FeCl3·2H2O]比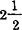 水合物的颜色更红。
水合物的颜色更红。
熔点73.5℃。
制法:
❶ 使浓盐酸与铁反应,制成氯化亚铁溶液,加热浓缩,再通入氯气,生成氯化铁溶液,然后浓缩及冷却结晶,可获得六水合物。再由六水合物制备其他水合物。
在100℃下向六水合物中通入氯化氢,则得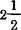 水合物,将
水合物,将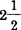 水合物熔化,则得无水物及二水合物。将无水物溶于3.75倍的水中,并结晶,可得
水合物熔化,则得无水物及二水合物。将无水物溶于3.75倍的水中,并结晶,可得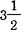 水合物。
水合物。
❷ 用硝酸氧化氯化亚铁,可制得[2]。
- 图尔浑欢詹是什么意思
- 图尔炳阿是什么意思
- 图尔玛是什么意思
- 图尔玛·嘉样端智是什么意思
- 图尔盖针茅是什么意思
- 图尔纳征是什么意思
- 图尔诺沃之战是什么意思
- 图尔达是什么意思
- 图尔都是什么意思
- 图尔额依格尔部是什么意思
- 图尔高是什么意思
- 图尤克喀拉别勒登窝孜峰是什么意思
- 图尤克沟是什么意思
- 图巴是什么意思
- 图巴古斯·普拉纳塔·蒂尔塔维查亚是什么意思
- 图巴尔拉克塔木是什么意思
- 图巴沟岛是什么意思
- 图布人是什么意思
- 图布升吉尔格勒是什么意思
- 图布德尼玛是什么意思
- 图布陛巴雅尔是什么意思
- 图布陞吉尔格勒是什么意思
- 图希是什么意思
- 图希海是什么意思
- 图帕克·阿马鲁是什么意思
- 图帖睦尔是什么意思
- 图幅是什么意思
- 图幛是什么意思
- 图库是什么意思
- 图库曼是什么意思
- 图库洛尔人是什么意思
- 图库洛尔帝国是什么意思
- 图库洛尔-法国战争是什么意思
- 图库鲁伊水电站是什么意思
- 图-底关系是什么意思
- 图度是什么意思
- 图廊是什么意思
- 图廊注记是什么意思
- 图开胜迹是什么意思
- 图式是什么意思
- 图式理论是什么意思
- 图弥三菩札是什么意思
- 图形是什么意思
- 图形与图象处理是什么意思
- 图形于影,未尽纤丽之容;察火于灰,不睹洪赫之烈是什么意思
- 图形公文是什么意思
- 图形凌烟阁是什么意思
- 图形分类是什么意思
- 图形加密是什么意思
- 图形卡片是什么意思
- 图形后效是什么意思
- 图形命名是什么意思
- 图形商标是什么意思
- 图形指认是什么意思
- 图形文字是什么意思
- 图形显示是什么意思
- 图形的不变性和不变量是什么意思
- 图形的分割与拼合是什么意思
- 图形的基本特征是什么意思
- 图形符号是什么意思